量子力学:将它们放在一起
同时,通过放射性进行发现,物理学家和化学家正在研究如何光与物质互动。这些研究开始了量子力学并帮助解决了原子的结构。
量子力学阐明了原子:Bohr模型
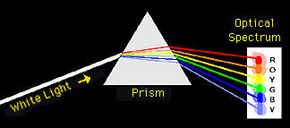
物理学家和化学家研究了光当电流通过含有气体元件(氢,氦,霓虹灯)的试管中,当元素在火焰中加热(例如钠,钾,钙等)时,就脱离了。他们通过光谱仪(一种包含狭窄缝隙和玻璃棱镜的设备)从这些源传递了光。
广告

照片由NASA提供
现在,当您将阳光传递到棱镜中时,您将获得像彩虹一样连续的颜色。但是,当这些各种来源的光经过棱镜时,他们发现了带有离散线条的黑暗背景。

照片由NASA提供

照片由NASA提供
每个元素都有一个独特的频谱波长光谱中的每一行的能量(请参阅光的工作原理有关波长和能量之间关系的详细信息)。
1913年,一位丹麦物理学家叫Niels Bohr将卢瑟福的发现与观察到的光谱一起提出了一个新的原子模型,以真正的直觉飞跃。Bohr建议,绕原子绕的电子只能在距核的一定能级(即距离)上存在,而不是在卢瑟福模型所期望的那样连续水平。当气管中的原子吸收了电流的能量时,电子变得兴奋,并从低能水平(靠近细胞核)跳到高能级(离核远方)。激发的电子将降回其原始水平,并以光作为光发出能量。由于能级之间存在特定的差异,因此在光谱中仅看到光的特定波长(即线)。
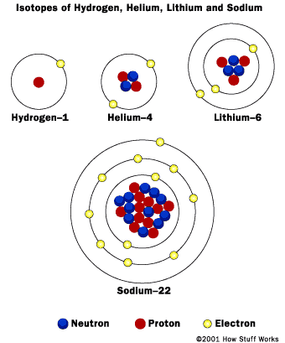
Bohr模型的主要优点是它起作用。它解释了几件事:
原子光谱 - 上面讨论
元素的周期性行为 - 具有相似特性的元素具有相似的原子光谱。
- 每个相同尺寸或能量的电子轨道(壳)只能容纳这么多电子。例如,第一个外壳可以容纳两个电子,第二个电子可以容纳8个电子,第三个电子可以容纳18个电子,第四个32,依此类推,直到达到第七个。
- 当填充一个外壳时,发现电子的水平较高。
- 化学特性基于最外壳中的电子数量。带有全外壳的元素不会反应。其他元素会占用或放弃电子以获得完整的外壳。
事实证明,Bohr的模型也可用于解释行为激光,尽管这些设备直到20世纪中叶才发明。
Bohr的模型是量子力学的新发现之前的主要模型。